服务假单胞菌遗传操作工具开发,推动基因表达基础和应用研究
相关菌株:Pseudomonas oleovorans T9AD=MCCC 1A04326
服务背景:假单胞菌属(Pseudomonas)包含革兰氏阴性菌中最大的属之一,广泛存在于从土壤、水体到极端环境的各种生境中。鉴于其代谢多样性,这些细菌在工业、农业和环境应用中展现出显著的潜力。作为一个鲜有致病性关联报道的成员,食油假单胞菌(Pseudomonas oleovorans)在烷烃降解和生物聚合物(如聚(3-羟基烷酸酯))生物合成方面表现出强大的能力,因此引起了相当大的生物技术关注。随后的研究揭示了该物种的更多功能,包括卤代除草剂的降解、甾体生物转化,不溶性锌盐的增溶,以及相容的溶质合成。这些发现进一步拓展了食油假单胞菌在除草剂生物修复、生物肥料开发、药物合成和保湿剂生产等方面的生物技术相关性。鉴于食油假单胞菌在除草剂生物修复、生物肥料开发、药物合成和保湿剂生产等方面的用途。一个方便、稳定的基因操作系统对于深入研究上述功能的遗传、生化和调控机制以及推进基因工程研究至关重要。然而,关于食油假单胞菌的专门方法和遗传工具的报道仍然非常有限。这些研究中的大多数依赖于为具有良好特征的物种(如恶臭假单胞菌)开发的方法(例如接合)。
服务对象:中国科学院青岛生物能源与过程研究所
取得成效:研究团队利用海洋衍生菌株T9AD (=MCCC 1A04326),建立了一个基于电转化的食油假单胞菌遗传操作系统。
食油假单胞菌 T9AD 抗生素敏感性:清晰的抗生素敏感性分析是开发特定微生物基因操作工具的基础,因为它指导选择性标记和工具载体的合理选择。为了确定食油假单胞菌 T9AD 的抗生素敏感性谱,使用了八种常用抗生素,即 Km、Amp、Cm、Spe、Apr、Gm、Neo 和 Stp,其终浓度高达 100 μg/mL,以施加选择压力(图1, A)。在液体培养中,Km 和 Gm 对细胞生长表现出最强的抑制作用。5 μg/mL的浓度即可完全抑制食油假单胞菌 T9AD 的生长,表明其最小抑制浓度(MIC)为 ≤5 μg/mL。相比之下,Stp、Apr、Neo 和 Spe 显示出中等程度的抑制。在抗生素浓度为 20 μg/mL(对于 Apr、Neo 和 Stp)或 50 μg/mL(对于 Spe)时观察到细胞生长被完全抑制。对于 Amp 和 Cm,在测试条件下未检测到抑制作用。在固体培养中也观察到了类似的抑制模式。
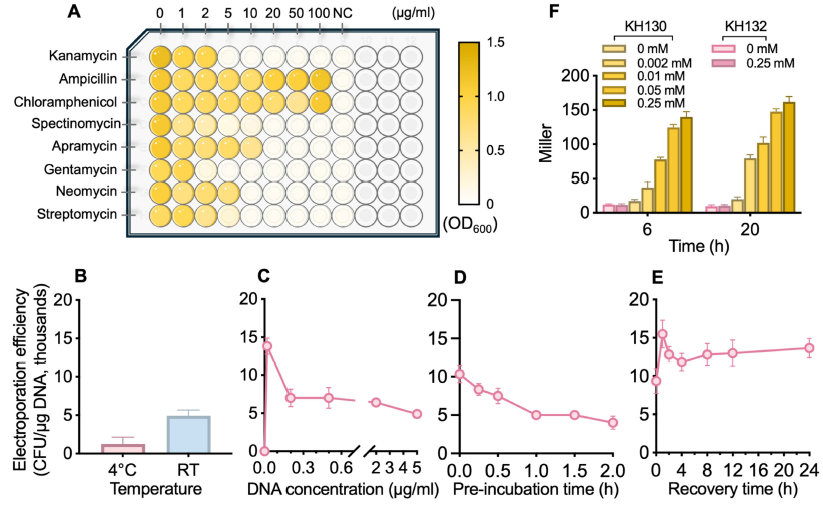
图1. 食油假单胞菌 T9AD 抗生素敏感性谱的测定(A),其电转化效率的优化以(B-E)及其中基于质粒的基因表达评估(F)
食油假单胞菌T9AD的电转化优化:将外源 DNA 导入假单胞菌细胞的最常用方法是接合和电转化。采用自杀载体和穿梭载体,遗传学组件被导入食油假单胞菌细胞,成功实现基因失活、染色体破坏、报告基因表达和基因互补。初步尝试T9AD的电转化其效率仅为66.7 CFU/ug DNA,远低于有效基因操作的水平。通过转化温度、质粒DNA浓度、预培养时间和恢复时间等4个参数优化电转化率。发现室温较4度更利于提高T9AD的转化效率(图1, B);质粒DNA浓度在0.2 ug/mL时可达最高转化效率,随后0.2 ug/mL时转化效率急剧下降(图1, C);不经过DNA-细胞预培养阶段转化效率更高(图1, D);脉冲后细胞恢复采用无抗生素培养基有利于提高转化效率(图1, E)。综合采用上述优化条件,T9AD的电转化效率达到104 CFU/ug DNA,能够满足如基因失活和表达等遗传操作。
在质粒平台上的可控基因表达:采用穿梭载体pBBR1MCS系列质粒可在T9AD中稳定自主复制。进一步使用该质粒通过大肠杆菌trc启动子(Ptrc)在 T9AD 菌株中驱动可诱导的 lacZ 报告基因表达。质粒转化后,在重组菌株 KH130 中观察到 lacZ 表达的剂量依赖性诱导(图1, F)。这些结果验证了基于 pBBR1MCS 的载体和 trc 启动子在食油假单胞菌中可控表达非天然基因的实用性。考虑到食油假单胞菌对 Km、Apr、Spe、Stp 和四环素敏感(图1, A),其他携带适当抗性盒的 pBBR1MCS 变体(例如 pBBR1MCS-2 和 pBBR1MCS-3)也可应用。除了广宿主范围能力外,pBBR1MCS 质粒还与其他来自 IncP、IncW 和 IncQ 组的广宿主范围质粒表现出良好的相容性。这一特性对合成生物学研究特别有用,因为它使得能够使用来自不同不相容群的质粒灵活地共表达多个基因或途径。
食油假单胞菌基因组中性平台的开发:基因组中性位点(NSs)是细菌遗传和代谢工程研究的有用工具。在这些染色体位点插入基因不会引起细胞可检测的表型变化。分析了 T9AD 菌株的基因组,选定了NS1(POT9AD_2766-2,767)和 NS2(POT9AD_5113-5,114)来研究其中性。通过同源重组将 Kmr基因和 Gmr基因分别独立引入这些位点(图2, A)。所得突变体 KH115、KH116、KH121 和 KH122 表现出预期的抗生素抗性。无论培养基是否含有 5% NaCl,突变菌株的生长均与野生型菌株相当(图2, B, C)。这表明外源基因整合到 NS1 和 NS2 并不影响食油假单胞菌 T9AD 的基本生长及其耐盐性。进一步研究发现在 NS1 和 NS2 的基因插入不影响食油假单胞菌的葡萄糖基甘油(glucosylglycerol, GG)合成代谢(图2, D)。
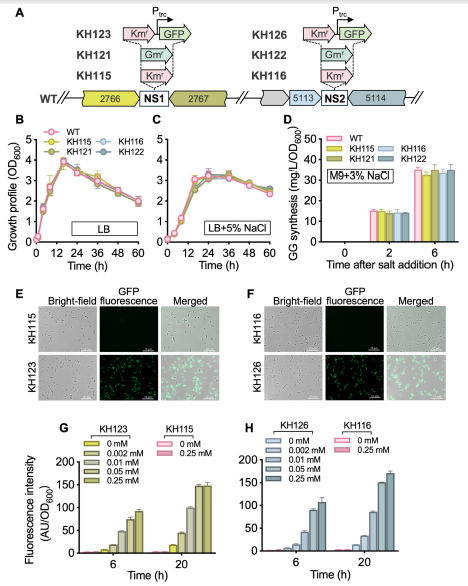
图2. 食油假单胞菌 T9AD 基因组中性位点的研究
与基于质粒的基因表达相比,基因组整合系统无需考虑质粒丢失、质粒不相容性和宿主范围限制。为了研究 NS1 和 NS2 的可行性,将绿色荧光蛋白报告基因(gfp)在 trc 启动子控制下整合到这些位点(图2, A)。在荧光显微镜下,重组菌株 KH123 和 KH126 显示出强烈的荧光,表明 gfp 表达成功(图2, E, F)。荧光强度与增加的 IPTG 浓度(0 至 0.25 mM)和诱导时间(6 至 20h)呈正相关(图2, G, H)。在相同条件下,对照菌株(KH115 和 KH116)未检测到 GFP 信号(图2, E-H)。这些结果表明,通过 NS1 和 NS2 平台内的 trc 调控系统,可以实现非天然基因或途径的稳定且剂量依赖性的表达。
结论:本研究为具有生物技术潜力的食油假单胞菌建立了一个基于电转化的遗传系统。氨基糖苷类抗生素,特别是 Km 和 Gm,对细胞生长显示出强效抑制作用,为选择性标记的设计提供了合理依据。通过优化细胞制备和电转化的温度、DNA浓度以及脉冲后细胞恢复,电转化效率提高到稳定达到 ∼104 CFU/μg∼104 CFU/μg DNA 的水平。利用广宿主范围载体 pBBR1MCS-5,可以实现基于质粒的外源基因可诱导表达。此外,开发并验证了两个基因组中性位点(NS1 和 NS2)用于基因整合,且无重大表型影响。总而言之,这些工具与已建立的接合方法一起,建立了一个强大的技术平台,以促进食油假单胞菌进一步的基础和应用研究。
(参考文献)Ke H, Zhang Z, Liu Y, Luo Q, Lu X. Development of genetic manipulation tools for Pseudomonas oleovorans. Front Microbiol. 2025 Oct 30;16:1691967.
汇编:Li G.
如有任何问题,请随时联系liguangyu@tio.org.cn
